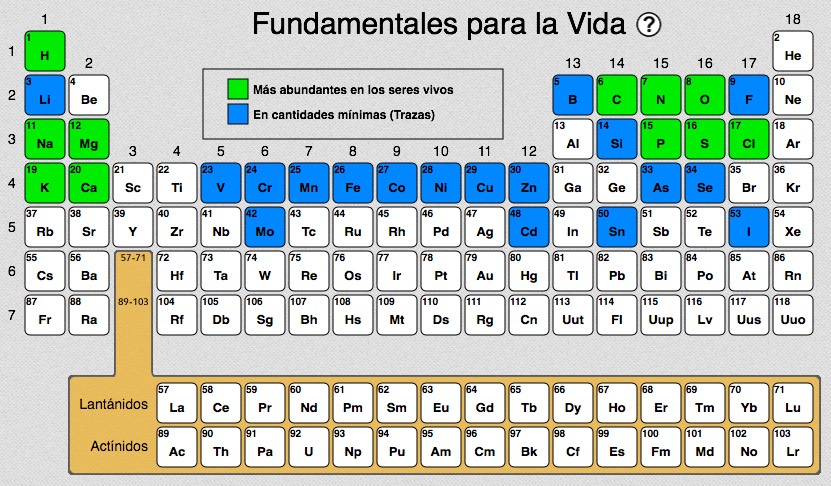
La tabla periódica esta compuesta actualmente por 118 elementos pero no siempre fue así, tuvieron que pasar muchos años para que los científicos lograran identificar cada elemento. En ese proceso pudieron, además, clasificarlos en varias caterorias en base a su número atómico, masa atómica, su origen, metales, no metales y los que son necesarios para la vida, incluida la nuestra. La siguiente información fue elaborada por la UNAM la cuál también puede ser encontrada en este enlace donde se ofrece además la posibilidad de ver las carácteristicas de los elementos de la tabla periódica.
Número atómico
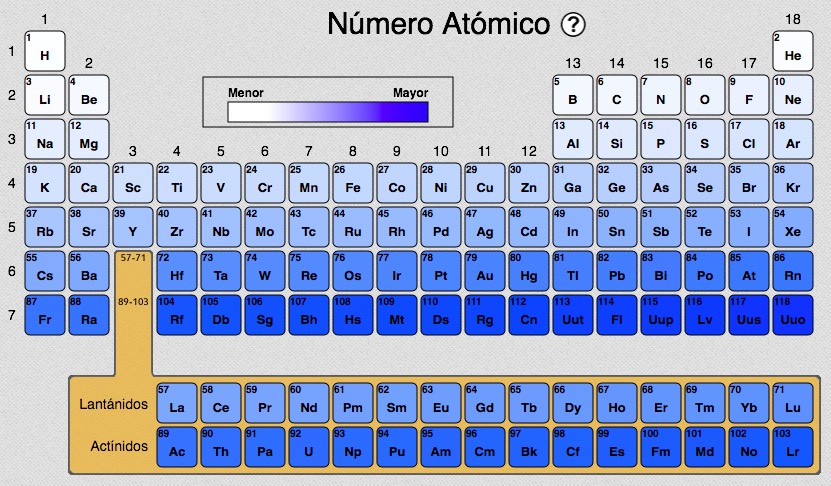
Cada elemento se distingue de los demás por el número de protones que tiene dentro del núcleo. La cantidad de neutrones o de electrones puede variar sin que el elemento pierda sus propiedades, pero con un protón de más o de menos ese elemento se convertirá en otro distinto.El número de protones de un elemento se conoce como número atómico.
Masa atómica
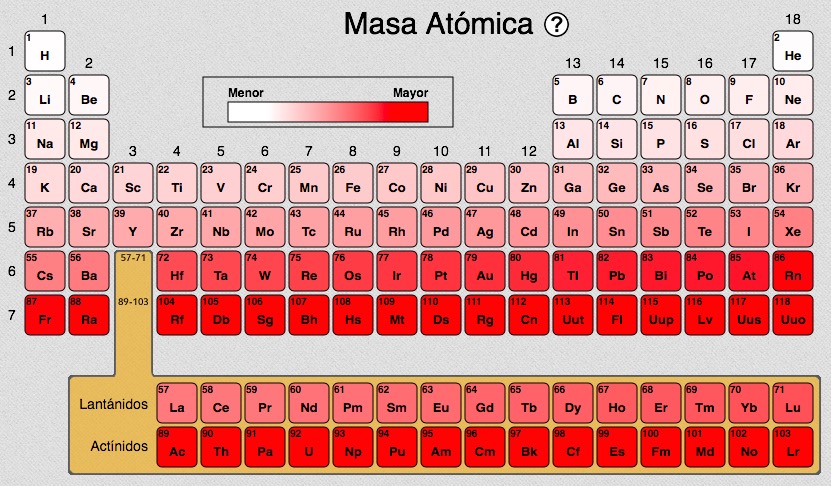
La suma de los neutrones y los protones que se encuentran dentro del núcleo se conoce como número de masa, que no es lo mismo que la masa atómica. Como puedes observar, la masa atómica casi nunca es un número entero. Lo que sucede es que existen átomos de un mismo elemento, conocidos como isótopos, con diferentes números de neutrones que por lo tanto tienen un número de masa distinto. El valor que se reporta en la Tabla Periódica es el número de masa promedio de los isótopos de cada elemento, que se conoce como masa atómica.Otro aspecto importante de notar es que los electrones no influyen en la masa atómica. Recuerda que la masa de un electrón es casi 1850 veces más pequeña que la de un protón, por lo que el núcleo concentra el 99.9% de la masa del átomo.
Clasificación según su origen
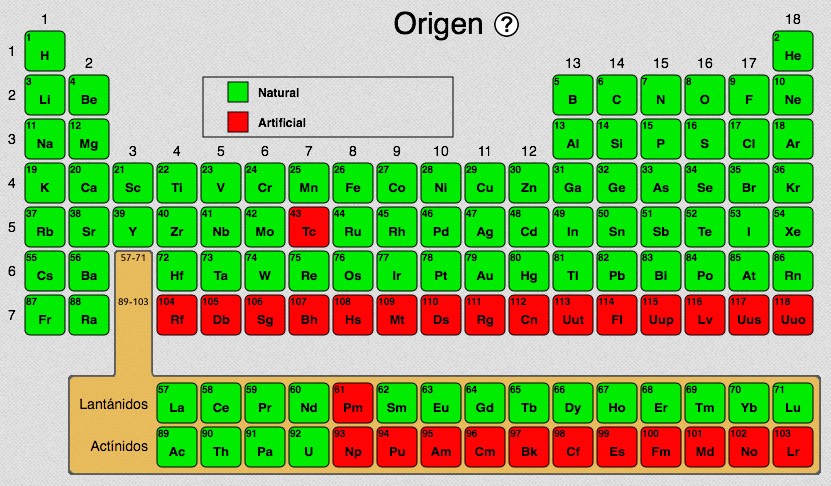
Según la teoría más aceptada del origen del universo, la mayoría de los elementos se formaron mediante procesos de fusión nuclear que iniciaron con el Big Bang. Se supone que existía una enorme concentración de partículas elementales, que explotaron liberando una gran cantidad de energía.El primer elemento que se formó fue el hidrógeno (H), que tiene un solo protón. Con las temperaturas tan alas que se alcanzaron, los átomos de H se unieron formando átomos de helio (He), que se unieron con otros para formar elementos cada vez más pesados. Este proceso sigue elementos cada vez más pesados. Este proceso sigue sucediendo en los núcleos de las estrellas jóvenes. En el Sol ya casi no se forman elementos pesados porque su temperatura ha disminuido, pero originalmente se formaron al menos 90, desde el hidrógeno hasta el uranio (U). Al desprenderse la Tierra hace millones de años, estos elementos llegaron a su corteza, con dos excepciones: El tecnecio (Tc) -primer elemento sintético- y el prometio (Pm), que si bien no se hallan en la Tierra, sí ha sido posible ubicarlos en algunas estrellas a través de su espectro electromagnético.Los elementos más pesados que el uranio (U) han sido sintetizados en laboratorios experimentales mediante aceleradores de partículas y procesos de fusión nuclear provocados por el hombre. Algunos de ellos tienen una vida media muy pequeña, de apenas algunos milisegundos.
Carácter metálico
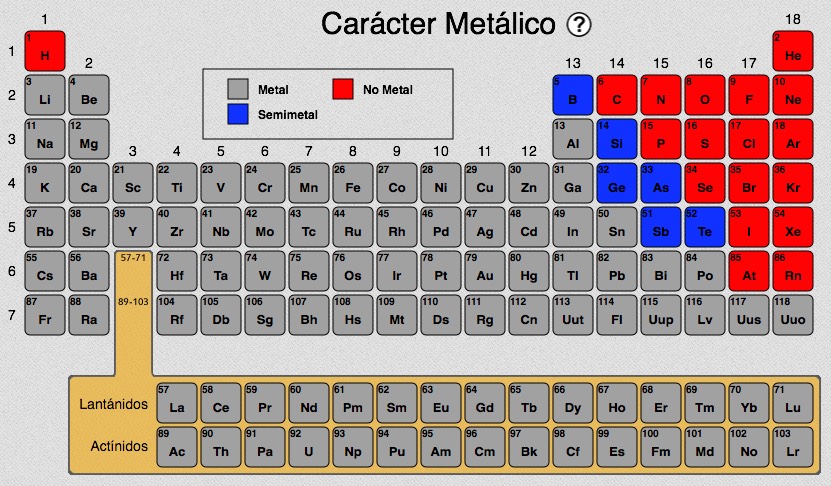
Desde el punto de vista químico un elemento se considera metal cuando cede fácilmente electrones y no tiene tendencia a ganarlos. Si observas la Tabla periódica notarás que los elementos metálicos se encuentran acomodados hacia la izquierda, ya que son los que tienen uno, dos o tres electrones en la última capa. Claro hay una excepción: el hidrógeno (H), porque es un gas y no puede considerarse metal.Por el contrario, los no metales están ubicados hacia la derecha porque en su última capa tienen seis o siete electrones y tienden a robarse los electrones de otros elementos. Evidentemente, los elementos del grupo 18 tienen completa la última capa y no interactúan con otros elementos, ni cediendo ni ganando electrones.Desde un punto de vista físico, los elementos metálicos presentan brillo, conducen el calor y la electricidad y son maleables.Observa que algunos elementos están señalados como “semimetales”. Lo que pasa en que en ocasiones se comportan como metales, pero bajo ciertas circunstancias no lo hacen. Algunos químicos incluyen en este grupo al astato y otros no.
Estado de agregación

En la tabla se muestra el estado de agregación de los elementos cuando no están sometidos a temperaturas o presiones extremas. La mayoría se encuentran en estado sólido y existen algunos gases. Sólo hay tres líquidos: el Mercurio (Hg) (cuyo símbolo se deriva de la expresión latina “Hydrargyrum” que significa “plata líquida”), el Boro (B) y el Francio (Fr). Este último es muy inestable: su vida promedio es de 22 minutos antes de convertirse en astato, que es un sólido.A partir del elemento 104 es muy difícil determinar el estado de agregación. Se trata de elementos sintetizados en laboratorio y sólo se han obtenido cantidades sumamente pequeñas que no permiten determinar con certeza la relación que tendrían sus átomos entre sí. Además, prácticamente no se ven: su vida media es de aproximadamente .0.25 milisegundos.
Fundamentales para la vida
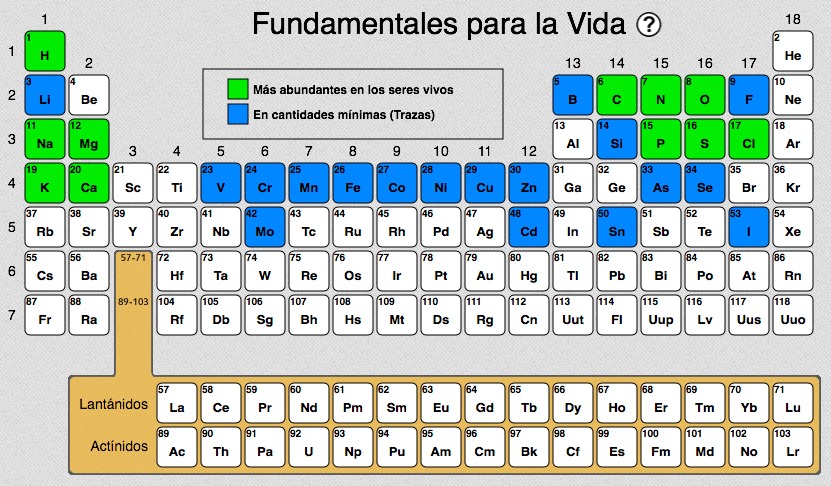
El 99% de la masa de cualquier ser vivo está formado por una colección muy pequeña de elementos: carbono (C), hidrógeno (H), oxígeno (O), nitrógeno (N), sodio (Na), magnesio (Mg), potasio (K), calcio (Ca), fósforo (P), azufre (S) y cloro (Cl). Con toda seguridad, este grupo de elementos es esencial para la vida.De los elementos que están marcados en azul, los químicos y los biólogos no están tan seguros de que sean esenciales, tal vez con la excepción del yodo (I). En los organismos vivos se encuentran en muy poca proporción, apenas algunas trazas y es muy difícil establecer qué pasaría si se suprimieran del todo en un organismo